 |
 |
 Em última análise, as ideias científicas não só devem ser testáveis, como também devem ser realmente testadas — de preferência através de múltiplas linhas de evidência e por muitas pessoas diferentes. Esta característica está no centro de toda a ciência. Os cientistas procuram ativamente evidência para testar as suas ideias — mesmo que o teste seja difícil e signifique, por exemplo, passar anos a trabalhar numa única experiência, viajando para a Antártica para medir os níveis de dióxido de carbono no gelo, ou recolhendo amostras de ADN de milhares de voluntários em todo o mundo. A realização de tais testes é muito importante para a ciência, porque na ciência, a aceitação ou rejeição de uma ideia científica depende da evidência que é relevante para a ideia — não do dogma, da opinião popular ou da tradição. Na ciência, as ideias que não são apoiadas pela evidência acabam por ser rejeitadas. E ideias que são protegidas de serem testadas, ou que só estão autorizadas a serem testadas apenas por um grupo com interesse no resultado, não podem ser consideradas como boa ciência.
Em última análise, as ideias científicas não só devem ser testáveis, como também devem ser realmente testadas — de preferência através de múltiplas linhas de evidência e por muitas pessoas diferentes. Esta característica está no centro de toda a ciência. Os cientistas procuram ativamente evidência para testar as suas ideias — mesmo que o teste seja difícil e signifique, por exemplo, passar anos a trabalhar numa única experiência, viajando para a Antártica para medir os níveis de dióxido de carbono no gelo, ou recolhendo amostras de ADN de milhares de voluntários em todo o mundo. A realização de tais testes é muito importante para a ciência, porque na ciência, a aceitação ou rejeição de uma ideia científica depende da evidência que é relevante para a ideia — não do dogma, da opinião popular ou da tradição. Na ciência, as ideias que não são apoiadas pela evidência acabam por ser rejeitadas. E ideias que são protegidas de serem testadas, ou que só estão autorizadas a serem testadas apenas por um grupo com interesse no resultado, não podem ser consideradas como boa ciência.
 |
 |
 |
Para aprender mais sobre a experimentação levada a cabo por grupos de interesse especiais e como isso pode inadvertidamente conduzir a favoritismos (e a má ciência), veja também Quem paga a ciência?
|
|
 |
 |
 |
 |
 |
 |
 |
UM MODELO DA CIÊNCIA:
RUTHERFORD E O ÁTOMO |
O laboratório de Ernest Rutherford testou a ideia de que a massa positiva de um átomo está distribuída difusamente, bombardeando um pedaço de uma folha de ouro com um feixe de partículas alfa, mas a evidência resultante desta experiência foi uma autêntica surpresa: a maioria das partículas alfa atravessou a folha de ouro tal como esperado, mas algumas destas partículas foram refletidas na direção oposta, como se tivessem atingido algo denso e sólido na folha de ouro. Se a massa dos átomos de ouro estivesse realmente distribuída de forma difusa, todas as partículas alfa deveriam ter passado através da folha de ouro, mas não o fizeram!
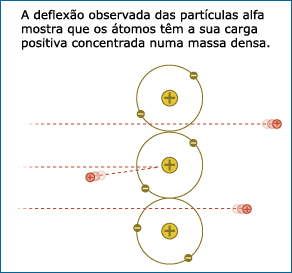
Através desta evidência, Rutherford concluiu que o modelo de bolo de passas do átomo estava incorreto, apesar de ser popular entre outros cientistas. Em vez disso, a evidência sugeria que um átomo é constituído maioritariamente por espaço vazio, e que a sua carga positiva está concentrada numa massa densa no seu centro, formando o núcleo. Quando as partículas alfa carregadas positivamente foram atiradas contra a folha de ouro, a maioria passou através do espaço vazio dos átomos de ouro com uma pequena deflexão, mas algumas delas foram de encontro ao núcleo denso de um átomo de ouro, carregado positivamente, sendo repelidas de volta para trás (tal como acontece se tentarmos que os polos positivos de dois ímanes fortes se toquem). A ideia que os átomos possuem um núcleo carregado positivamente também era testável. Muitas experiências independentes foram conduzidas por outros investigadores para ver se a ideia se encaixava com outros resultados experimentais.
A história de Rutherford continua à medida que analisamos cada um dos itens descritos no guia da ciência. Para saber mais como esta investigação se integra com o resto dos itens, continue a ler.
|
 |
 |
 |
 |
 |
|
 |
|
 |
 |
